Corpo de conhecimentos (BOK: body of knowledge), norma, modelo e framework de processos
flexM4I > abordagens e práticas > Corpo de conhecimentos (BOK: body of knowledge), normas, padrões e frameworks de processos (versão 2.2)
Autoria: Henrique Rozenfeld([email protected])
Corpo de conhecimentos (BOK)
Definição
Corpo de conhecimentos (BOK – body of knowledge, em inglês) é uma compilação de conhecimentos criada por algumas organizações para que os profissionais da área de conhecimento, que essas organizações representam, possam usar como referência na sua profissão. Essa compilação pode estruturar: conceitos, termos, princípios, práticas, processos, atividades, padrões e templates. Essas organizações podem ser associações de classes ou profissionais, instituições representativas de um segmento empresarial, órgãos normativos etc.
| No nosso glossário você pode consultar outras definições de BOK |
Exemplos de BOKs
- o do Instituto de Gestão de Projetos (PMI), denominado Corpo de Conhecimentos em Gestão de Projetos (PMBOK)
- o da Associação para Gestão de Projetos (APM), denominado BOK da APM (APM BOK)
- o do Conselho Internacional de Engenharia de Sistemas (INCOSE), denominado BOK da Engenharia de Sistemas (SEBok: system engineering BOK)
- o da Associação de Profissionais de Gestão de Processos de Negócio (ABPMP), denominado corpo comum de conhecimentos (CBOK), que é um guia para gerenciamento de processos de negócio
- o do Instituto Internacional de Análise de Negócios (IIBA), denominado Corpo de Conhecimentos de Análise de Negócio (BABOK), que é um guia para análise de negócios
Na wikipedia em inglês você pode encontrar mais exemplos de BOKs.
Normas, padrões ou regulamentos para inovação
Definição
Segundo o nosso glossário …
Normas (padrões) são documentos, estabelecidos por consenso e aprovados por um órgão reconhecido, que fornecem, para uso comum e repetido, regras, diretrizes ou características para atividades ou seus resultados, visando atingir o grau ótimo de ordem em um determinado contexto.
Regulamentos são atos administrativos, relacionados a uma norma, com objetivo de especificar o que diz uma lei ou dispor situações que ainda não foram disciplinadas por ela. Um regulamento também é denominado de regulamentação.
|
Regulamentação tem dois sentidos: 1) é o ato regulamentar de emitir normas ou regulamentos; 2) o resultado deste ato, regulamento, também é denominado de regulamentação. Consulte os seguintes termos no glossário para esclarecer as diferenças entre eles: regulamentação, regulação, regulamento, padrão, padronização, norma e normalização. |
Exemplos de padrões, normas e regulamentos
Padrões para gestão da inovação e projetos
Algumas organizações chamam a compilação de práticas de padrões / normas (standards). Exemplos:
- padrão de gestão de portfólio do PMI
- padrões de gestão de projetos do IPMA (International Project Management Association)
Algumas dessas organizações são instituições normativas, como a ABNT, ISO, DIN, e publicam normas, que podem ser utilizadas como referência. Exemplos:
- diretrizes para gestão da inovação, ISO 56002:2019 innovation management system – guidance;
- ABNT NBR ISO 56000:2021 – Gestão da inovação – Fundamentos e vocabulário
- ABNT NBR ISO 56003:2021 – Gestão da inovação – Ferramentas e métodos de parceria para a inovação – Orientações
- ABNT NBR ISO 56002:2020 – Gestão da inovação – Sistema de gestão da inovação – Diretrizes
- série de normas ISO 21500:2021 em gestão de projetos
- Princípios de solução para o desenvolvimento metódico de produtos, DIN – VDI 2222 Blatt1
- Diretrizes para incorporação do ecodesign – dentro dos sistemas de gestão ambiental, ISO 14006:2020
- Seção 8.3 da norma de requisitos do sistema de gestão de qualidade da, ABNT NBR ISO 9001
Normas
Seguem alguns exemplos de normas da área de construção civil:
- NBR 6118 – Projeto de estruturas de concreto – Procedimento
- NBR 6136 – BLocos vazados de concreto simples para alvenaria – Requisitos
- NBR 7199 – Projeto, aplicação e execução de vidros
- NBR 7678 – Procedimentos para garantir condições de segurança e higiene no canteiro de obras
- NBR 13.531 – Elaboração de projeto de edificações – Atividades técnicas
- NBR 15.575 – Desempenho de edificações habitacionais
|
Entre no site da ABNT e veja o catálogo de normas técnicas existente. Entre na “Pesquisa Avançada” e veja se não existe alguma norma técnica que a sua empresa precisaria cumprir. Por exemplo, uma busca na data de hoje, fevereiro de 2023, resultou:
Trouxemos 5 exemplos, que correspondem a normas de 5 comitês técnicos. A ABNT possui 336 comitês técnicos. |
Exemplos de regulamentações da indústria farmacêutica
Vamos listar alguns exemplos extraídos do guia de desenvolvimento de fármacos da FDA (food and drug administration) do governo dos USA e da ANVISA (Agência Nacional de Vigilância Sanitária) do governo brasileiro.
FDA – Q8 (R2) para regulamentar o desenvolvimento de drogas
Q8( R2) princípios do quality by design (QbD): abordagem sistemática de desenvolvimento de drogas com ênfase no entendimento do produto e processo, assim como controle do processo baseado na gestão do risco de qualidade.
- QTPP (quality target product profile): sumário qualitativo das características de uma droga que idealmente será atingido para assegurar a qualidade desejada, considerando segurança e eficácia
- CQA (critical quality attributes): propriedades ou características físicas, químicas, biológicas e microbiológicas, que devem estar dentro de um limite apropriado para assegurar a qualidade desejada do produto
- CPP (critical process parameter): parâmetro do processo (de fabricação), cuja variabilidade tem um impacto no CQA e, portanto, deve ser monitorado e controlado para assegurar que o processo produz a qualidade desejada (CQA)
- CMA (critical material attributes): propriedades ou características físicas, químicas, biológicas e microbiológicas da matéria prima, que devem estar dentro de um limite apropriado para assegurar a qualidade desejada do produto (CQA)
Existem ainda outras normas a serem consideradas, tais como a ICH Q9 quality risk management e a ICH Q10 pharmaceutical quality system). Essas normas estão disponíveis neste link.
ANVISA – RDCs para regulamentar o desenvolvimento de medicamentos
RDCs (resolução de diretoria colegiada) orientam o uso obrigatório de normas para regulamentar o desenvolvimento de drogas. Consulte a lista de normas relacionadas a medicamentos. Existem tantas RDCs revogadas, que não é simples encontrar a norma atual em vigência.
Exemplos:
- Neste link está a RDC 497, que dispõe sobre os procedimentos administrativos para concessão de Certificação de Boas Práticas de Fabricação (CBPF) e de Certificação de Boas Práticas de Distribuição e/ou Armazenagem.
- Guia para elaboração de Arquivos Mestres de Plantas – AMP (Site Master File – SMF)
- Boas Práticas de Fabricação de Insumos Farmacêuticos Ativos.
ANVISA – Exemplos de regulamentações da indústria de alimentos
Para a indústria de alimentos existe na ANVISA uma biblioteca de normas, regulamentos e padrões que devem ser seguidos e exigem controles de processo específicos.
O HACCP (Hazard Analysis and Critical Control Points) é um sistema preventivo de controle da segurança dos alimentos, que considera todas as fases da cadeia alimentar.
ANVISA – Exemplos transversais
Normas e padrões de temas transversais são definidos para serem atendidos por mais de um setor.
| Neste link você pode consultar várias informações da ANVISA, que é responsável pela regulação dos seguintes produtos: alimentos, cosméticos, ensaios clínicos, medicamentos, produtos de cannabis, produtos para saúde, saneantes e tabaco. |
Normas e regulamentos delimitam a gestão da inovação
Os exemplos de norma que mostramos referem-se a aspectos de gestão da inovação. Mas, em cada área de aplicação existem muitas normas que devem ser consideradas, que vão além da gestão da inovação. São normas que padronizam especificações e características do objeto a ser desenvolvido.
Algumas normas, regulamentos e padrões devem ser obrigatoriamente considerados
Em alguns segmentos, como o de alimentação, bebidas, cosméticos, equipamentos médicos, farmacêutico e aeronáutico (por exemplo), existem normas e padrões que definem requisitos que devem ser atendidos. São determinados por legislação. Em alguns casos, os padrões são rigorosos e praticamente determinam algumas das atividades de inovação.
Por exemplo, o desenvolvimento de um novo fármaco deve seguir um padrão regulamentado pela ANVISA. Nas fases iniciais, de descoberta dos princípios ativos, não existe muita regulamentação. A partir desta descoberta, as demais fases de ensaios são regulamentadas. A fase de ensaios clínicos deve seguir a resolução da diretoria colegiada (RDC) número 9 de 2015 da ANVISA. Esta RDC define os procedimentos e requisitos para a realização de ensaios clínicos, incluindo a submissão do Dossiê de Desenvolvimento Clínico de Medicamentos (DDCM) a ser aprovado pela ANVISA.
Na maior parte das vezes, normas relacionadas a produtos e processos são mandatórias, se for em um setor regulamentado, e as empresas precisam cumprir os requisitos para poder homologar o resultado da inovação perante agências reguladoras ou empresas de certificação que avaliam se os produtos e processos seguem as especificações dos regulamentos e normas.
Modelo de processo e modelo de referência de processos
Definição
O termo modelo de processo é polissêmico o que causa muitas ambiguidades. Vamos adotar a seguinte definição: “Modelo de processo é uma representação de um processo de uma empresa específica”.
O termo modelo de referência de processos também é polissêmico. Vamos adotar a seguinte definição: “Modelo de referência de processo é uma representação de um processo genérico, independente de uma empresa específica”.
|
No glossário você encontra uma discussão mais completa sobre essas definições para entender a nossas escolhas: |
Consideramos também que um modelo de referência é um sinônimo de metodologia, que é um conjunto de métodos. Você pode utilizar uma ou mais metodologias para extrair os métodos mais adequados aos seus propósitos e, assim, compor um processo da sua empresa.
Mais a frente ilustramos essas definições, juntamente com o corpo de conhecimentos.
Exemplos
Na seção “Metodologias e modelos de processos” apresentamos exemplos de modelos de referência / metodologias e de modelos de processo / processos de algumas empresas (é difícil ter acesso e poder publicar modelos de processos de empresas).
Exemplo
Algumas associações denominam os BOKs que eles publicam de framework, como o framework de classificação de processos da APQC (American Productivity and Quality Center), que traz um modelo de referência de processos de negócio de uma empresa. Esse framework, em particular, apresenta uma estrutura hierárquica de processos, que uma empresa pode usar como referência para definir os seus processos.
Como utilizar os BOKs, padrões e normas?
Apresentamos alguns exemplos de objetivos para aplicar essas publicações, destacamos a importância da disciplina nas fases de detalhamento das inovações e mostramos como derivar um modelo de processo para a sua empresa, a partir dessas publicações.
Exemplos de objetivos de aplicação
Lógico que os objetivos de aplicação dependem dos usuários e papéis que eles possuem dentro das empresas, mas neste tópico listamos somente os objetivos.
Você pode usar essas publicações como referência na sua totalidade ou parcialmente. Por exemplo:
- você pode usar totalmente o conteúdo de uma publicação, porque ela traz requisitos que você é obrigado a atender para certificar seu produto, serviço, instalações ou para realizar um processo de acreditação de parte de sua empresa;
- você pode adotar parcialmente práticas de publicações para certificação profissional (típico de alguns BOKs) ou para complementar seus processos de inovação (por exemplo, com relação à gestão de projetos).
- algumas publicações trazem diretrizes detalhadas, que você pode transformar em procedimentos dos processos ou mesmo instruções de trabalho (por exemplo, as diretrizes obrigatórias para se especificar um cordão de solda para unir partes de vasos de alta pressão, assim como as instruções de inspeção, quando um processista estiver confeccionando um roteiro de fabricação / plano de trabalho – process plan).
- utilizar como benchmarking, uma especie de checklist, que você pode utilzar para verificar se está realizando as atividades ou aplicando as práticas, que são consideradas boas práticas em uma determinada área de aplicação;
- você terá de definir documentos de processo (formulários) para submeter sua inovação para certificação / aprovação de um cliente. Como por exemplo, na área automotiva, o documento padrão de FMEA (failure mode and effect analysis) da norma norma IATF 16969:2016 (que substituiu a ISO/TS 16949:2009 – https://www.iatfglobaloversight.org/ ).
- você tem de submeter a documentação de produto para atender aos requisitos da ANVISA para aprovar um equipamento médico ou um novo fármaco.
Esses casos anteriores, normalmente, estão relacionados com as fases de detalhamento ou certificação, que também fazem parte da inovação.
Além disso, essas publicações servem:
- para você aprender em como inovar / desenvolver algum produto ou processo;
- como uma referência para aprendizado da perspectiva de gestão;
- pode ser utilizado para definir níveis de maturidade de seus processos / negócios.
São importantes para as fases de detalhamento
Não pense que inovação é só o momento da inspiração !! As fases de detalhamento de um projeto de inovação são muito importantes para “fazer acontecer”, avaliar, homologar e certificar o que foi concebido nas fases iniciais.
Nas fases de detalhamento temos de manter a disciplina de um processo para garantir a repetibilidade e atender a possíveis requisitos de normas com o objetivo de homologar e/ou certificar a ofertas criadas ou os processos desenvolvidos.
|
O conhecimento documentado nessas publicações correspondem a possíveis capabilidades ordinárias que você pode adotar. Trazem um diferencial em mercados não desenvolvidos. Do contrário, é praticar o conhecimento comum (por isso que já está documentado). Para obter um diferencial, sua empresa precisa possuir as capabilidades dinâmicas. Leia mais sobre isso na seção “gestão da inovação e capabilidades da empresa”. |
Certificação de profissionais
Alguns BOKs são usados para certificar profissionais. Mas, normalmente, esses profissionais precisam cumprir outros requisitos para serem certificados. Exemplos:
- O BOK de gestão de projetos do PMI (project management institute) serve de referência para se obter um certificado de “profissional em gestão de projetos” (PMP: project management professional).
- A ABPMP (Association Of Business Process Management Professionals International) possui três programas de certificação de profissionais em BPM (business process management)
- O IIBA (International Institute of Business Analysis) possui alguns programas de certificação de profissionais, tais como: Agile Analysis Certification, Certified Business Analysis Professional, Certification in Business Data Analytics, Certificate in Cybersecurity Analysis, Certification of Capability in Business Analysis, Certificate in Product Ownership Analysis, Entry Certificate in Business Analysis (este ultimo baseado no BABOK – Business Analysis Body of Knowledge)
Como definir um modelo de processo da sua empresa a partir dessas publicações?
Um processo executado em uma empresa, que não esteja documentado / sistematizado / formalizado, pode ser analisado, talvez melhorado a partir da comparação com as publicações citadas e então documentado em um modelo de processo da sua empresa.
| Existem ainda um grande número de publicações de relatos de experiências profissionais, que podem ser consideradas neste contexto. |
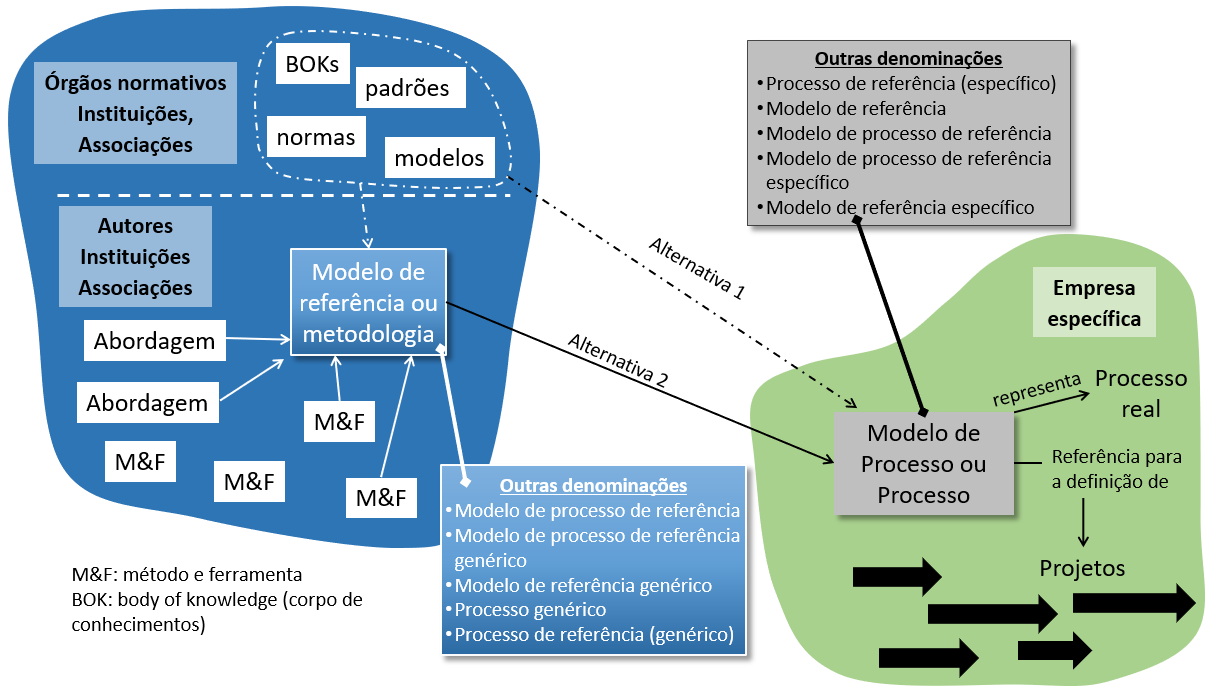
Existem duas outras alternativas para se utilizar essas publicações com o objetivo de definir um modelo de processo para a sua empresa (veja a próxima figura):
Figura 243: ilustração de duas alternativas para se definir um modelo de processo específico para uma empresa a partir BOKs, padrões e normas: 1) estudando os documentos; 2) instanciando (derivando) o processo a partir de um modelo de referência (genérico) – clique na figura para aumentá-la.
- Alternativa 1: sua empresa estuda essas publicações e incorpora no processo o que for necessário para atender aos requisitos exigidos ou para adotar as melhores práticas documentadas nessas publicações.
| Cuidado para não engessar o processo real. Você pode criar Instruções de trabalho, que podem se tornar informações adicionais a serem consideradas na execução dos processos. |
- Alternativa 2: Uma instituição (associação de classe, um autor, uma consultoria etc.) pode adotar e combinar práticas de diversos BOKs e abordagens para criar uma metodologia a ser usada como referência para empresas (normalmente de um segmento específico) definirem os seus processos. A empresa adota a referência e define seus processos a partir do conteúdo dessas referências, complementando com princípios de abordagens e práticas (métodos e ferramentas) extraídas de outras fontes.
|
Segundo Fettke et al. (2005), existem diversos atributos de um modelo de referência que podem ser utilizados para diferenciá-los. Um deles é o domínio do modelo de referência, que pode ser:
Existem ainda modelos de referência genéricos, chamados de universais pelos autores, que são bem amplos e, normalmente, estão documentados em livros. Na área de desenvolvimento de produtos, Gericke & Moser (2014) definiram quatro níveis de abstração de um modelo de processo (entre parênteses colocamos os termos que utilizamos na flexM4i):
|
Referências
Fettke, P., Loos, P., & Zwicker, J. (2005). Business process reference models: Survey and classification. Lecture Notes in Computer Science (Including Subseries Lecture Notes in Artificial Intelligence and Lecture Notes in Bioinformatics), 3812 LNCS, 469–483. https://doi.org/10.1007/11678564_44
Gericke, K. and Moser, H.A. (2014), “Adapting a Design Approach : A Case Study in a Small Space Company”, in Heisig, P. and Clarkson, P.J. (Eds.), Proceedings of the 2nd International Workshop on Modelling and Management of Engineering Processes.
ISO 1996. ISO, T. ISO/IEC Guide 2 “Standardization and related activities – General vocabulary”. International Organisation for Standardization / International Electrotechnical Commission, Geneva, 7th edition, 1996.
Penzenstadler, B., Fernandez, D. M., Richardson, D., Callele, D., & Wnuk, K. (2013). The requirements engineering body of knowledge (REBoK). 2013 21st IEEE International Requirements Engineering Conference, RE 2013 – Proceedings, 377–379. https://doi.org/10.1109/RE.2013.6636758